Кристалічні решітки в хімії
Зміст:
Визначення
Як ми знаємо, всі матеріальні речовини можуть перебувати в трьох базових станах: рідкому, твердому та газоподібному. Правда є ще стан плазми, який вчені вважають ні багато ні мало четвертим станом речовини, але наша стаття не про плазму. Твердий стан речовини тому твердий, оскільки має особливу кристалічну структуру, частки якої знаходяться в певному і чітко заданому порядку, створюючи, таким чином, кристалічну решітку. Будова кристалічної решітки складається з повторюваних однакових елементарних осередків: атомів, молекул, іонів, інших елементарних частинок, пов’язаних між собою різними вузлами.
Види решіток
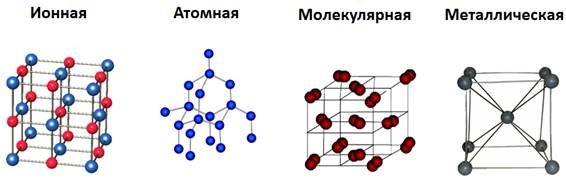
Залежно від частинок кристалічної решітки існує чотирнадцять її типів, наведемо найбільш популярні з них:
- Іонна кристалічна решітка.
- Атомна кристалічна решітка.
- Молекулярна кристалічна решітка.
- Металева кристалічна решітка.
Далі більш детально опишемо всі типи кристалічної решітки.
Іонна решітка
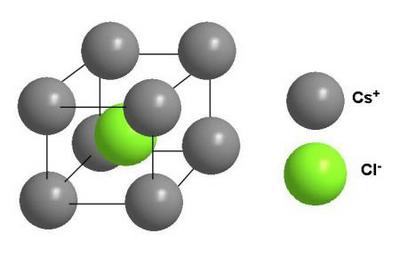
Головною особливістю будови кристалічної решітки іонів є протилежні електричні заряди, власне, іонів, внаслідок чого утворюється електромагнітне поле, яке визначає властивості речовин, що мають іонну кристалічну решітку. А це тугоплавкість, твердість, щільність і можливість проводити електричний струм. Характерним прикладом іонної кристалічної решітки може бути кухонна сіль.
Атомна решітка
Речовини з атомною кристалічною решіткою, як правило, мають у своїх вузлах, що складаються власне з атомів сильні ковалентні зв’язки. Ковалентний зв’язок відбувається, коли два однакових атома діляться один з одним по-братськи електронами, утворюючи, таким чином, загальну пару електронів для сусідніх атомів. Через це ковалентні зв’язки сильно і рівномірно пов’язують атоми в строгому порядку – мабуть, це найхарактерніша риса будови атомної кристалічної решітки. Хімічні елементи з подібними зв’язками можуть похвалитися своєю твердістю, високою температурою плавлення. Атомну кристалічну решітку мають такі хімічні елементи як алмаз, кремній, германій, бор.
Молекулярна решітка
Молекулярний тип кристалічної решітки характеризується наявністю стійких і щільноупакованих молекул. Вони розташовуються у вузлах кристалічної решітки. У цих вузлах вони утримуються такими собі вандервальсовими силами, які в десять разів слабкіше сил іонної взаємодії. Яскравим прикладом молекулярної кристалічної решітки є лід – тверда речовина, що має однак властивість переходити в рідку – зв’язки між молекулами кристалічної решітки зовсім слабенькі.
Металева решітка
Тип зв’язку металевої кристалічної решітки гнучкіше і пластичніше іонної, хоча зовні вони дуже схожі. Відмінною особливістю її є наявність позитивно заряджених катіонів (іонів металу) у вузлах решітки. Між вузлами живуть електрони, які беруть участь у створенні електричного поля, ці електрони ще називаються електричним газом. Наявність такої структури металевої кристалічної решітки пояснює її властивості: механічну міцність, тепло та електропровідність, плавкість.

Автор: Павло Чайка, головний редактор журналу Пізнавайка
При написанні статті намагався зробити її максимально цікавою, корисною та якісною. Буду вдячний за будь-який зворотний зв'язок та конструктивну критику у вигляді коментарів до статті. Також Ваше побажання/питання/пропозицію можете написати на мою пошту pavelchaika1983@gmail.com або у Фейсбук.
Ця стаття доступна англійською мовою – Crystal Lattice in Chemistry.

