Як розставляти коефіцієнти в хімічних рівняннях
Зміст:
Всі хімічні реакції, що проходять в навколишньому світі можна описати за допомогою спеціальних рівнянь, що представляють собою хімічні формули та математичні знаки з коефіцієнтами. І від правильно розставлених коефіцієнтів в хімічних рівняннях часом залежить не багато не мало, а те якою власне і буде хімічна реакція і чи буде вона взагалі. У нашій статті ми розповімо про те, як правильно розставляти коефіцієнти в хімії, щоб хімічні рівняння були записані вірно.
Приклад розбору простих реакцій
Головне правило, яким слід керуватися при складанні хімічних рівнянь – принцип збереження енергії речовини, тобто, скільки є атомів кожного хімічного елемента в лівій частині рівняння, стільки повинно бути і в правій частині того ж рівняння.
Для прикладу візьмемо хімічну реакцію взаємодії кальцію (Ca) з киснем (O2). Але для початку пояснимо, чому взагалі кисень (як і деякі інші хімічні елементи) в хімічних рівняннях записується з індексом «2». Справа в тому, що одна молекула кисню має 2 атома, тому його записують як O2. У свою чергу, наприклад, одна молекула води, що складається з кисню і водню, має всім відому формулу H2O. Це означає, що кожна молекула води складається з двох атомів водню і одного атома кисню. Зауважте, що на свій розсуд індекси в хімічних рівняннях і формулах міняти не можна, так як вони спочатку повинні бути написані правильно.
Тепер повернемося до нашого простого прикладу реакції взаємодії кальцію і кисню. Її можна записати наступним чином:
Ca + O2 → 2CaO
Про що говорить цей запис? Про те, що в результаті хімічної реакції взаємодії кальцію з киснем утворюється оксид кальцію, який записаний формулою CaO. Але також зверніть увагу, що в правій частині оксид кальцію ми записали з коефіцієнтом 2 – 2CaO. Це означає, що кожен з двох атомів кисню зчепився зі своїм атомом кальцію, але тоді маємо невідповідність – в правій стороні у нас два атома кальцію, в той час як в лівій тільки лише один. А значить, щоб запис був правильним в лівій частині ми повинні перед кальцієм поставити коефіцієнт 2:
2Ca + O2 → 2CaO
Тепер ми можемо перевірити наше рівняння – з лівого боку у нас два атома кальцію і з правого теж два, а значить між обома частинами можна цілком справедливо поставити знак рівності:
2Ca + O2 = 2CaO
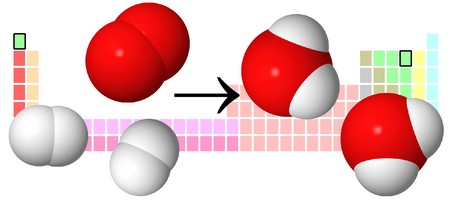
Розберемо ще один простий приклад, з взаємодії кисню і водню як ми знаємо, народжується одна з найцінніших і незвичайних речовин у Всесвіті (і це без перебільшення) – вода, основа життя на нашій планеті. Утворення води можна записати наступним рівнянням:
H2 + O2 → H2O
Але де ж тут закралася помилка? Давайте розберемо: в лівій частині у нас два атома кисню, а в правій тільки один. Значить перед формулою води необхідно поставити коефіцієнт 2:
H2 + O2 → 2H2O
Множення 2 молекул води на 2 атома водню дасть нам 4 атома водню з правого боку, але ж з лівого боку атомів водню лише два! Значить перед воднем в рівнянні ми також повинні поставити коефіцієнт 2 і тепер отримаємо правильне хімічне рівняння, де замість стрілочки → можна вже сміливо поставити знак рівності.
2H2 + O2 = 2H2O
Приклад розбору складної реакції
Тепер давайте розберемо те, як проставляти коефіцієнти в більш складних хімічних рівняннях:
NaOH + H2SO4 → Na2SO4 + H2O
Перед вами запис так званої реакції нейтралізації – взаємодія кислоти і основи, в результаті якого утворюються солі і вода.
Що ж ми маємо тут: з лівого боку у нас один атом натрію (Na), а з правого індекс говорить, що атомів натрію вже стало два. Значить логічно, що хімічну формулу основи гідроксиду натрію NaOH треба помножити на 2. Або іншими словами поставити перед нею коефіцієнт 2:
2NaOH + H2SO4 → Na2SO4 + H2O
Кількість сірки в сірчаній кислоті (H2SO4) і солі сульфаті натрію (Na2SO4) у нас однакова, тут все добре, а ось з кількістю кисню та водню знову невідповідність, з лівого боку кисню 6, а з правого 5. Водню з правого боку 4, а з лівого тільки 2, непорядок. Щоб правильно записати це хімічне рівняння треба зрівняти кількість кисню і водню в лівій і правій частині рівняння, на щастя тут зробити це просто, треба перед H2O поставити коефіцієнт 2.
2NaOH + H2SO4 = Na2SO4 + 2H2O
Таким чином, кількість всіх хімічних елементів в правій і лівій частині рівняння у нас зрівнялася, а значить, ми неспроста поставили знак рівності.
Для закріплення матеріалу розберемо ще один приклад складного рівняння.
Ba(OH)2 + HNO3 → Ba(NO3)2 + H2O
Це рівняння відображає хімічну реакцію гідроксиду барію (Ba(OH)2) з азотною кислотою (HNO3) в результаті якої утворюється нітрат барію (Ba(NO3)2) і вода.
Приклад цей нам цікавий тим, що тут використовуються дужки. Вони означають, що якщо множник стоїть за дужками, то кожен елемент множиться на нього. Почнемо ж розбирати це рівняння, перше, що кидається в очі, невідповідність азоту N, зліва він один, а ось праворуч, якщо брати до уваги дужки, його вже два. Отримаємо наступне:
Ba(OH)2 + 2HNO3 → Ba(NO3)2 + H2O
Тепер у нас зліва стало 4 атома водню, а праворуч тільки 2. Значить, перед формулою води також ставимо коефіцієнт 2.
Ba(OH)2 + 2HNO3 = Ba(NO3)2 + 2H2O
Тепер всі елементи зрівняні, і ми справедливо поставили знак рівності.

Автор: Павло Чайка, головний редактор журналу Пізнавайка
При написанні статті намагався зробити її максимально цікавою, корисною та якісною. Буду вдячний за будь-який зворотний зв'язок та конструктивну критику у вигляді коментарів до статті. Також Ваше побажання/питання/пропозицію можете написати на мою пошту pavelchaika1983@gmail.com або у Фейсбук.

